阿尔茨海默病(AD)是导致痴呆的首要原因,其病理特征之一是大脑中淀粉样蛋白斑块的沉积。长期以来,“淀粉样蛋白级联假说”主导着AD的药物研发,大量资源被投入到清除细胞外Aβ斑块上。然而,靶向细胞外Aβ的疗法屡屡受挫,提示我们需要重新审视Aβ的神经毒性机制。近年来,越来越多的证据表明,神经元内部的Aβ积累是AD病理发生中更早期的关键事件,它甚至发生在细胞外斑块形成和神经炎症之前。
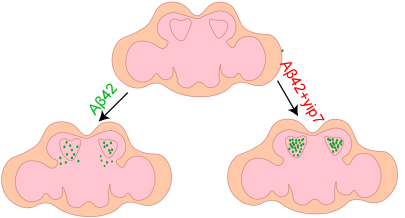
2026年3月18日,《Advanced Science》在线发表了题为“Intracellular Aβ42 Sequestration by a Serine Protease Mitigates Neurotoxicity in a Drosophila Alzheimer’s Disease Model”的研究论文。该研究利用果蝇AD模型,发现一种名为Yip7的丝氨酸蛋白酶能通过在神经元内结合并“滞留”Aβ42蛋白来有效减轻其神经毒性。研究团队发现,神经元过表达Yip7有效缓解了由Aβ42诱导的多重神经毒性缺陷,包括运动能力下降、蛋白质稳态失衡、脑老化加速、神经元死亡以及寿命缩短。Yip7能够直接与细胞内的Aβ42结合,将其“滞留”在神经元内部,导致神经元内Aβ蛋白总量增加。这种“滞留”作用意外地显著降低了Aβ对机体的毒性。Yip7蛋白的作用机制为未来药物设计提供了一个新颖的切入点,即通过模拟Yip7的功能,设计能够追踪并“困住”细胞内Aβ的分子。该研究不仅拓展了对丝氨酸蛋白酶功能的认识,也为开发针对细胞内淀粉样蛋白的治疗策略提供了新思考。
湖南师范大学翟宗昭教授和吴葩教授为共同通讯作者,博士生苏静云为论文第一作者,杨猛、王歆锋参与了部分工作。该研究得到了国家自然科学基金、湖南省自然科学基金及湖南省优势特色学科群项目资助。
论文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202517862
